Au vu de la persistance des ruptures d’approvisionnement des médicaments à base de flécaïnide à libération prolongée, l’ANSM a publié une nouvelle recommandation spécifique aux patients souffrant des maladies cardiaques héréditaires ou rares suivantes :
- tachycardies ventriculaires polymorphes catécholaminergiques ;
- certaines formes de syndrome de QT long congénital ;
- cardiomyopathies arythmogènes dont cardiomyopathie ventriculaire droite arythmogène (DVDA).
Estimés à près de 1000, ces patients particulièrement vulnérables font l’objet d’un suivi par des centres de référence et des centres de compétence des maladies rares (CCMR) dont la liste est disponible ici.
En l’absence de flécaïnide à libération prolongée mettant en jeu le pronostic vital de ces patients et à défaut d’alternative thérapeutique, il vous est demandé de ne réaliser aucune substitution et de suivre le protocole décrit ci-après.
Prescription au patient
Pour la prescription de flécaïnide à libération prolongée, chaque CCMR remet à son patient une lettre explicative accompagnée des trois documents suivants :
- une ordonnance nominative,
- une lettre des laboratoires BIOGARAN et VIATRIS SANTE (Annexe 1),
- un document nominatif d’accompagnement du CCMR et du prescripteur (Annexe 2).
Délivrance par le pharmacien d’officine
Les laboratoires BIOGARAN et VIATRIS SANTE ont accepté, à la demande de l’ANSM, de réserver un stock spécifique de boites de Flécaïnide LP 50 mg, 100 mg, 150 mg et 200 mg pour répondre aux besoins des patients.
En pratique, un patient suivi par un CCMR se rend dans votre officine et vous présente les trois documents précités :
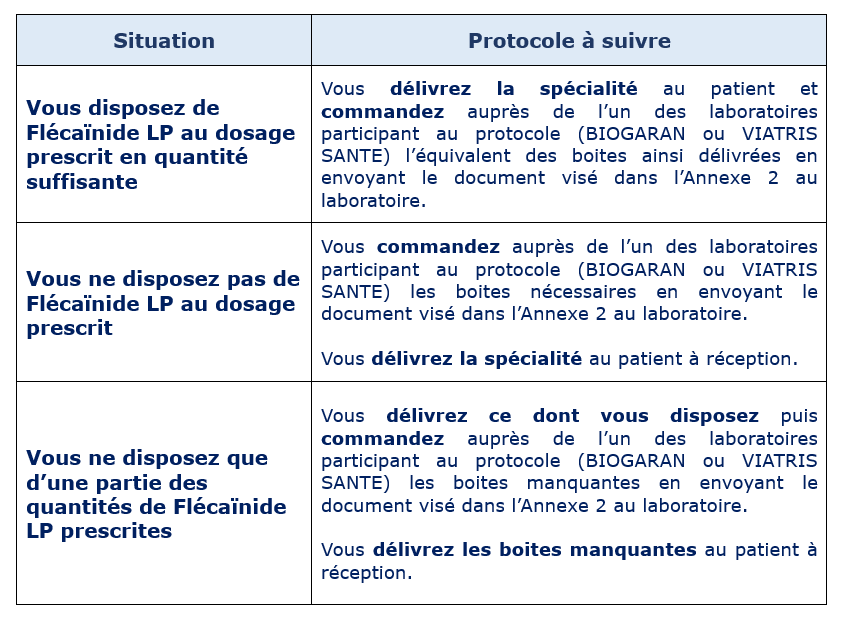
En outre, vous pouvez consulter :
- Le courrier d’information de l’ANSM à destination des pharmaciens d’officine.
- Le protocole spécifique à la délivrance de Flécaïnide aux patients souffrants de maladies cardiaques graves.
